Verlässliche ERP-Prozesse unterstützen Regulatory Affairs
Sicherheit für Medtech & Pharma mit Microsoft Dynamics 365
Verlässliche ERP-Prozesse unterstützen Regulatory Affairs
Eine exzellente Datenbasis ist das Rückgrat der Medtech-Branche. In diesem Artikel erfahren Sie, warum eine validierungsfähige ERP-Lösung für Hersteller oft wichtiger ist als reine Regulatory Affairs Software-Inseln und wie Sie die Anforderungen an Prozesssicherheit und Rückverfolgbarkeit erfüllen. Erfahren Sie, wie Sie nicht nur die Dokumentation sauber halten, sondern durch Innovation und Automatisierung Ihre Effizienz steigern.
Lückenlose Rückverfolgbarkeit und Datensicherheit
Der Einsatz spezialisierter Systeme ist für Unternehmen unverzichtbar. Oft liegt der Fokus dabei auf Regulatory Affairs Software, doch ohne ein integriertes ERP-System fehlen die entscheidenden Daten.
- Durch manuelle Pflege von Information (Excel/Papier) entstehen Inkonsistenzen. Dies führt zu Risiken bei Audits und potenziellen Verzögerungen bei der Markteinführung (Time-to-Market).
- Die strengen Normen und Regularien verlangen lückenlose Rückverfolgbarkeit von Materialien und Prozessen, die ohne integriertes System kaum zu bewältigen sind.
- Um Issues schnell zu identifizieren, benötigen Sie eine vernetzte Datenbasis. Isolierte Tools erschweren die Validierung und die Sicherheit.
Dies sind Herausforderungen, die Schweizer Medtech-Firmen täglich beschäftigen. Die ERP-Lösung Microsoft Dynamics 365 Business Central bietet die Technologie, die als Fundament für jedes QMS unerlässlich ist.

Was leistet eine validierungsfähige ERP-Software?
Eine ERP-Software für die Medizintechnik fungiert als zentrale Datenquelle. Sie ist die Basis, auf der spezialisierte Regulatory Affairs Software aufsetzen kann. Sie ist die zentrale Plattform, die technische Voraussetzungen mitbringt, um in einem regulierten Umfeld validiert zu werden – etwa im Kontext der FDA 21 CFR Part 11. Dies umfasst die Unterstützung für elektronische Records und Signaturen, welche die Datenintegrität gewährleisten.
Dies ermöglicht es, den Lebenszyklus Ihrer Produkte digital zu dokumentieren. Auch für die Pharma-Branche bietet diese Technologie entscheidende Vorteile und ist eines der wichtigsten Tools für Compliance.
Branchenspezifische Konfigurationen sind für Schweizer Unternehmen wichtig, um lokale Gesetze effizient abzubilden. Die Software lenkt den Warenfluss und liefert Daten für die korrekte Kennzeichnung.
Zu den Kernfunktionen gehören die Chargenverfolgung sowie die Verwaltung von Seriennummern für Medizinprodukte. Diese Funktionen gewährleisten, dass Sie jederzeit auskunftsfähig sind. Damit leisten Sie einen wesentlichen Beitrag zur Qualität und Produktsicherheit.
Wichtige Funktionen für Medtech-Unternehmen
Unsere Lösung bietet Features, die speziell auf die Unterstützung von GxP-Themen ausgelegt sind.
Das System unterstützt zudem die Umsetzung der Computer System Validation (CSV), indem es dokumentierte Abläufe liefert. Aproda agiert hierbei als Partner, der hilft, den Validierungsaufwand zu reduzieren. Wir bringen fundiertes Praxiswissen ein, damit Ihr Team im Alltag sicher agieren kann.
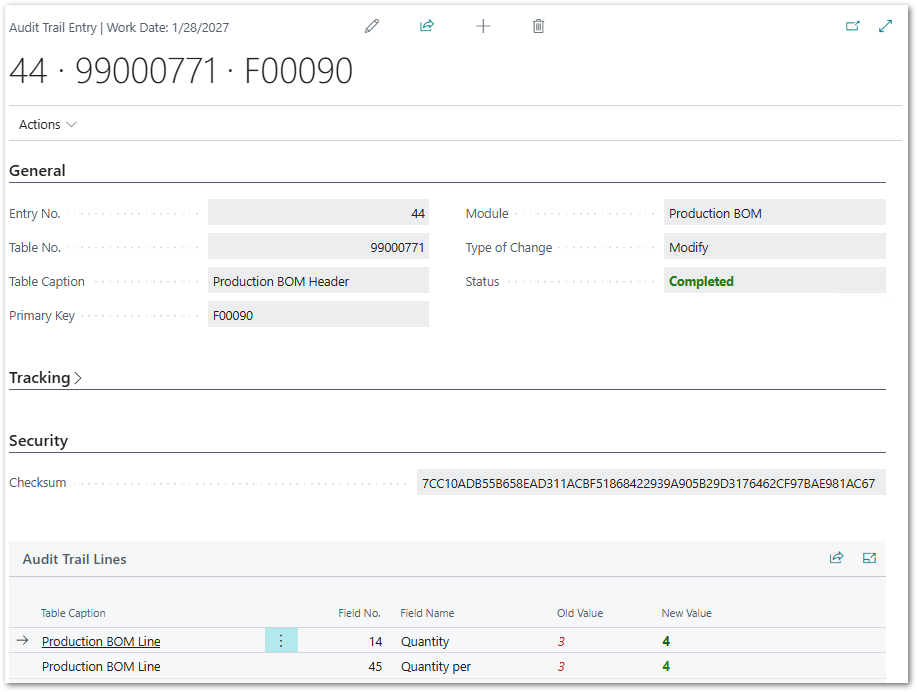
Rückverfolgbarkeit & Traceability, Audit Trail
End-to-End Transparenz vom Rohstoff bis zum Warenausgang
- Lückenlose Rückverfolgbarkeit über alle Fertigungsstufen
- Bi-Direktionale Chargenrückverfolgung für maximale Sicherheit
- Historie aller Warenbewegungen im Audit Trail
- Sperrlagerverwaltung und Quarantäne-Status Management (Checks)
- Eindeutige Identifikation von Chargen und Seriennummern
Qualitätsmanagement Support (QMS)
Integration von Prüfschritten in die Logistik
- Qualitätsmanagement direkt im ERP-System integriert (Keine Datensilos)
- Verwaltung von Prüfmitteln (Equipment) im ERP-Kontext
- Datenbereitstellung für Ihr externes QMS (Qualitätsmanagementsystem)
- Unterstützung bei der Einhaltung von Standard Operating Procedure (SOP)
- Lieferantenbewertung als wichtiger Part der Qualitätssicherung
Dokumentenmanagement & Records
Stammdaten als Basis für die Compliance
- Zentrale Verwaltung von Artikelstammdaten und Produkte-Informationen
- Versionierung von Stücklisten und Rezepturen
- Verknüpfung von Dokumenten mit Artikeln
- Sichere Datenbank für elektronische Aufzeichnungen (Records)
- Unterstützung der Daten-Integrity durch Änderungsprotokolle
Supply Chain & Produktion
Validierungsfähige Abläufe und Resilienz
- Produktionsplanung unter Berücksichtigung von Ressourcen
- Fremdfertigungssteuerung (Verlängerte Werkbank/externe Produktion)
- Digitale Prozesse in der Fertigung
Supply Chain Resilienz durch intelligentes Bestandsmanagement
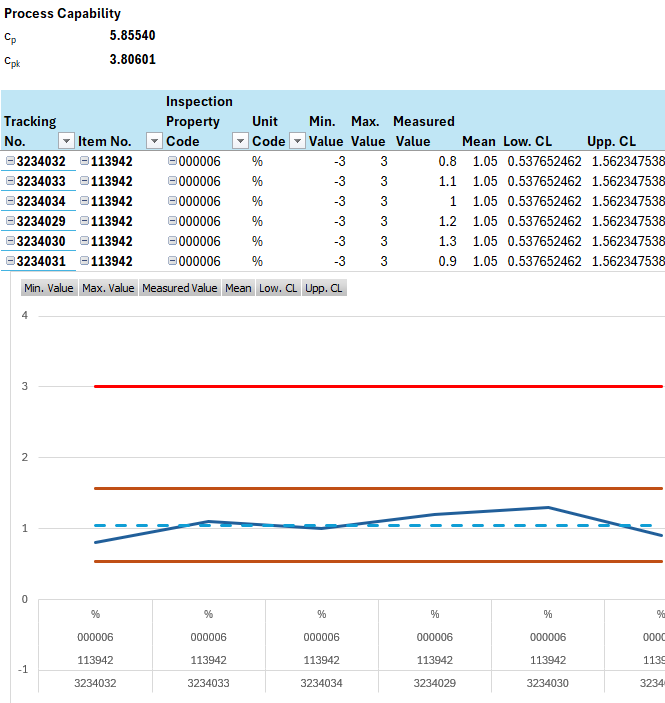
Reporting & Business Intelligence/ Analyse
Daten für fundierte Entscheidungen
- Dashboards zu Lagerbeständen und Lieferfähigkeit
- Kennzahlen zur Lieferantentreue und Quality
- Schnelle Datenbereitstellung für unangekündigte Audits
- Überblick über die aktuelle Situation in jeder Form
Validierung und Compliance Sicherheit
Die Validierung ist für Medtech-Unternehmen Pflicht. Ein System wie Microsoft Dynamics 365 Business Central reduziert den Aufwand, da es als Standardsoftware etablierte Prozesse mitbringt. Wichtig: Business Central ist eine validierungsfähige Software, die wir in Ihre Systemlandschaft integrieren. Dies unterscheidet sie von starrer Regulatory Affairs Software.
Weitere Vorteile unserer Lösung sind:
- die Unterstützung bei Audits durch schnelle Datenverfügbarkeit.
- die klare Rolle des ERP als führendes System für Bewegungsdaten.
- die Vermeidung von Fehlern in kritischen Themen.
- der Fokus auf skalierbares Wachstum für verschiedene Branchen der Life Sciences.
Dies ist der sichere Weg zu einer stabilen IT-Infrastruktur.
Vorteile der Implementierung
Zusammengefasst bietet die spezialisierte Software die notwendige Sicherheit für moderne Companies.
Jederzeit auskunftsfähig. Alle Buchungshistorien sind sofort abrufbar. Ideal für die Vorbereitung auf Prüfungen.
Verkürzen Sie Ihre Time-to-Market durch geordnete Datenstrukturen.
Systemseitige Sperren verhindern, dass gesperrte Produkte in der Produktion verwendet werden.
Standardisierte Processes vom Einkauf bis zum Verkauf sorgen für Fehlerreduktion.
Wir liefern Grundlagen und Dokumentationen, um die Validierung der ERP-Software effizient durchzuführen. Wir bieten Ihnen hierbei volle Unterstützung.
Ob Start-up oder Konzern – die Lösung wächst mit und deckt den Bedarf nach Stabilität ab.
Das bietet das ERP System für Medizintechnik
- Validierungsfähige Basis für Strukturierte Abläufe für GxP-Konformität
- Lückenlose Traceability vom Lieferanten bis zum Versand – vollständige Transparenz
- Integrierte Standards Berücksichtigung gängiger Normen und Vorgaben
- Schnelle Bereitstellung Cloud-ERP oder On-Premise
- Intuitive Nutzung hohe Akzeptanz durch moderne Oberfläche
- Investitionsschutz Zukunftssichere Technologie von Microsoft
Patrick Glauser | Sales Executive Microsoft ERP
Sehr gern berate ich Sie persönlich. Rufen Sie mich an:
058 200 14 14 oder schreiben Sie mir ein E-Mail. Ich freue mich auf Ihre Kontaktaufnahme!
Häufig gestellte Fragen
Was unterscheidet ERP von Regulatory Affairs Software?
Regulatory Affairs Software ist oft auf die Verwaltung von Zulassungen spezialisiert. Das ERP-System hingegen liefert die operativen Daten (Chargen, Mengen, Herstellnachweise), die für die Compliance zwingend notwendig sind.
Was bedeutet validierungsfähige Software?
Eine validierungsfähige Software bietet technische Voraussetzungen (wie Audit Trail, Versionierung), um validiert zu werden. Business Central ist nicht vorab validiert, sondern wird im Rahmen des Projektes für den spezifischen Einsatzzweck validiert.
Unterstützt das System FDA 21 CFR Part 11?
Das System bietet technische Features wie Protokollierung von Änderungen und Zugriffskontrollen (Controls), die eine wichtige Voraussetzung für die Einhaltung von Signatures und elektronischen Records Anforderungen darstellen.
Ist ein vollständiges QMS enthalten?
Business Central ist ein ERP-System. Es unterstützt QMS-relevante Prozesse (z.B. Wareneingangsprüfung), ersetzt aber kein spezialisiertes CAQ-System, sondern liefert diesen Systemen die notwendigen Stammdaten.
Wie wird die Kennzeichnung gelöst?
Die Stammdaten für Etiketten werden zentral im ERP gepflegt. Für den physischen Druck binden wir spezialisierte Drittlösungen über Schnittstellen an, um die Kennzeichnung normgerecht umzusetzen.
Wie unterstützt das System die UDI-Pflicht?
Das ERP-System verwaltet zentral alle UDI-relevanten Stammdaten (Device Identifier und Production Identifier). Es generiert automatisch die korrekten Barcodes via integrierter Labeling-Software und stellt Schnittstellen bereit für GUDID Datenbank Export.
Kann ich meine bestehenden Qualitäts-Prozesse integrieren?
Absolut. Das integrierte CAQ‑Modul lässt sich flexibel an bestehende Qualitäts‑ und Prüfpläne anpassen. Ihre aktuellen SOPs – im Sinne von Arbeitsplänen, Arbeitsanweisungen oder Prüfschritten – können vollständig digital im System abgebildet werden. Dadurch wird die korrekte Prozessausführung automatisch sichergestellt.
Auf Wunsch lassen sich diese Workflows zusätzlich durch Power Automate erweitern, z. B. für Freigabeprozesse, Benachrichtigungen oder Eskalationen. So ersetzen Sie mühsame Excel‑Listen durch klare, geführte und revisionssichere Abläufe – und steigern die Effizienz Ihres Qualitätsmanagements nachhaltig.
Wie hilft Aproda bei der Validierung?
Aproda verfügt über Erfahrung und unterstützt Sie bei der Erstellung der notwendigen Dokumente und der Tests. Wir begleiten Sie bei Fragen rund um die Validierung der ERP-Prozesse und bieten umfassenden Support.
Warum Aproda AG
Seit 1983 begleiten wir KMUs auf dem Weg in die Digitalisierung. Wir verstehen die Sprache der MedTech-Branche und transformieren Ihre Compliance-Bedürfnisse in funktionierende IT-Lösungen. Unser Fokus liegt auf der Sicherheit Ihrer Produkte.
- Verständnis für Regulierungs-Standards
- Erfahrung mit Validierungsprojekten
- Schweizer Partner für lokale Services
- Qualität & Verfügbarkeit von unserem Support
- Ganzheitliche Betrachtung von IT und Prozessen


